Das Salz, richtiger das „Kochsalz“, das bei uns im Museum vorgestellt wird, ist nur ein Salz unter vielen.
Zur Unterscheidung von anderen Salzen benennt es der Chemiker nach seinen beiden Bestandteilen „Natriumchlorid“ oder kurz „NaCl“.
Chlor ist ein gelbgrünes giftiges Gas, das zum Beispiel zur Desinfektion benutzt wird. Sein Geruch ist aus Schwimmbädern bekannt.
Natrium ist ein ebenso gefährliches Gift. Es ist ein Metall, das bei Berührung mit Luft oder Wasser heftig reagiert.
Giftige Stoffe im Essen?
Nein, denn als chemische Verbindung verlieren Natrium und Chlor ihre Gefährlichkeit. Natriumchlorid zeigt ganz andere Eigenschaften als seine Bestandteile. Es besteht wie alle Salze aus elektrisch geladenen Teilchen – den Ionen. Das Natrium liefert dem Chlor negativ geladene Teilchen und wird dadurch zum positiv geladenen Natrium-Ion. Das Chlor nimmt die negative Ladung auf und wird zum negativ geladenen Chlorid-Ion. Beide sind vergleichsweise harmlose Teilchen.
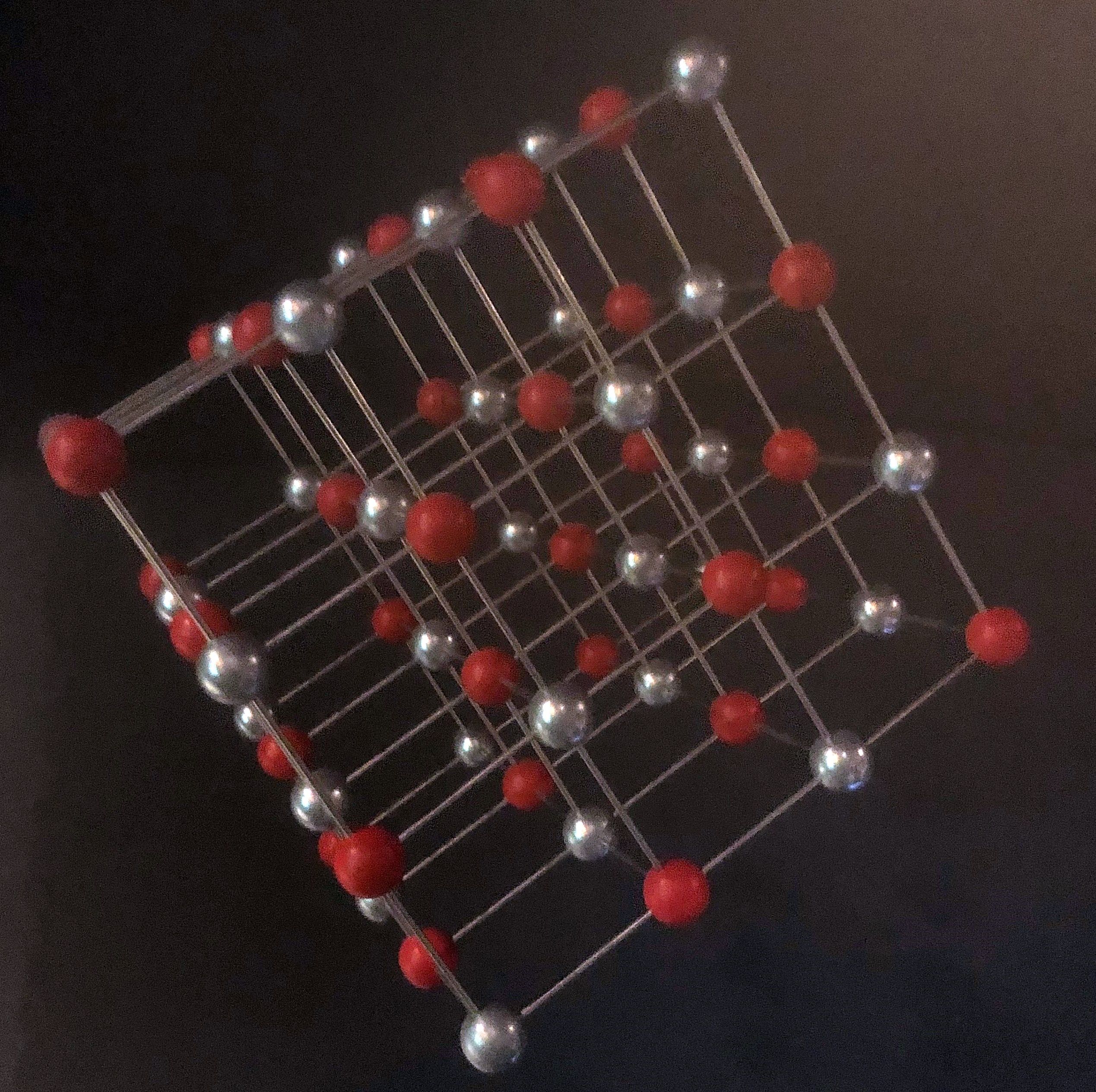
Die entgegengesetzt geladenen Ionen ziehen sich gegenseitig an. Dabei wirken ihre Anziehungskräfte nicht nur in eine bestimmte, sondern in alle Richtungen. Es entsteht ein regelmäßig aufgebautes Ionengitter, in dem jedes Natrium-Ion von sechs Chlorid-Ionen und jedes Chlorid-Ion von sechs Natrium-Ionen würfelförmig umgeben ist.
Da alle Ionen immer auf die gleiche Weise angelagert werden, zeigt sich die würfelförmige Anordnung der Natrium- und Chlorid-Ionen auch in der äußeren Form der Kochsalzkristalle:
Die Kristalle sind Würfel. Häufig wachsen sie treppenförmig zu hohlen Pyramiden an.